DNA dizilimi için kullanılan mevcut teknikler, büyük bir hücre grubundaki nadir genetik mutasyonların tespit edilmesini sağlayacak hassasiyete sahip değiller. Mutasyonun gözlemlenmesi, örneğin kanserin erken teşhis edilmesi konusuda büyük öneme sahip.
Genetik araştırmalar
Kral Abdullah Bilim ve Teknoloji Üniversitesi’nden (KAUST) bilim insanları tarafından oluşturulan bir ekip, yakın bir zamanda “Tekli DNA Moleküllerinin Dizilimi” (IDMseq) olarak bilinen bir teknik geliştirdi. Söz konusu teknoloji, 10 bin hücrelik bir gen grubu içerisinde tek bir gen mutasyonunun bile doğru bir şekilde tespit edilmesini sağlıyor.
Birbirine bağlı moleküllerin iki zincirinden meydana gelen DNA bir çift sarmal yapı oluşturuyor. Tüm genetik veriler bu çift sarmalın üzerine kaydediliyor. Bu sebeple de hayatın genetik kodu olarak adlandırılıyor.
Ekibin çalışmaları ile ilgili bir diğer önemli nokta da insanlardaki embriyonik kök hücrelerde, CRISPR-Cas9 gen düzenleme tekniğinin sebep olduğu mutasyonların sayısını ve sıklığını belirlemek için IDMseq teknolojisini kullanılmasının başarılması oldu.
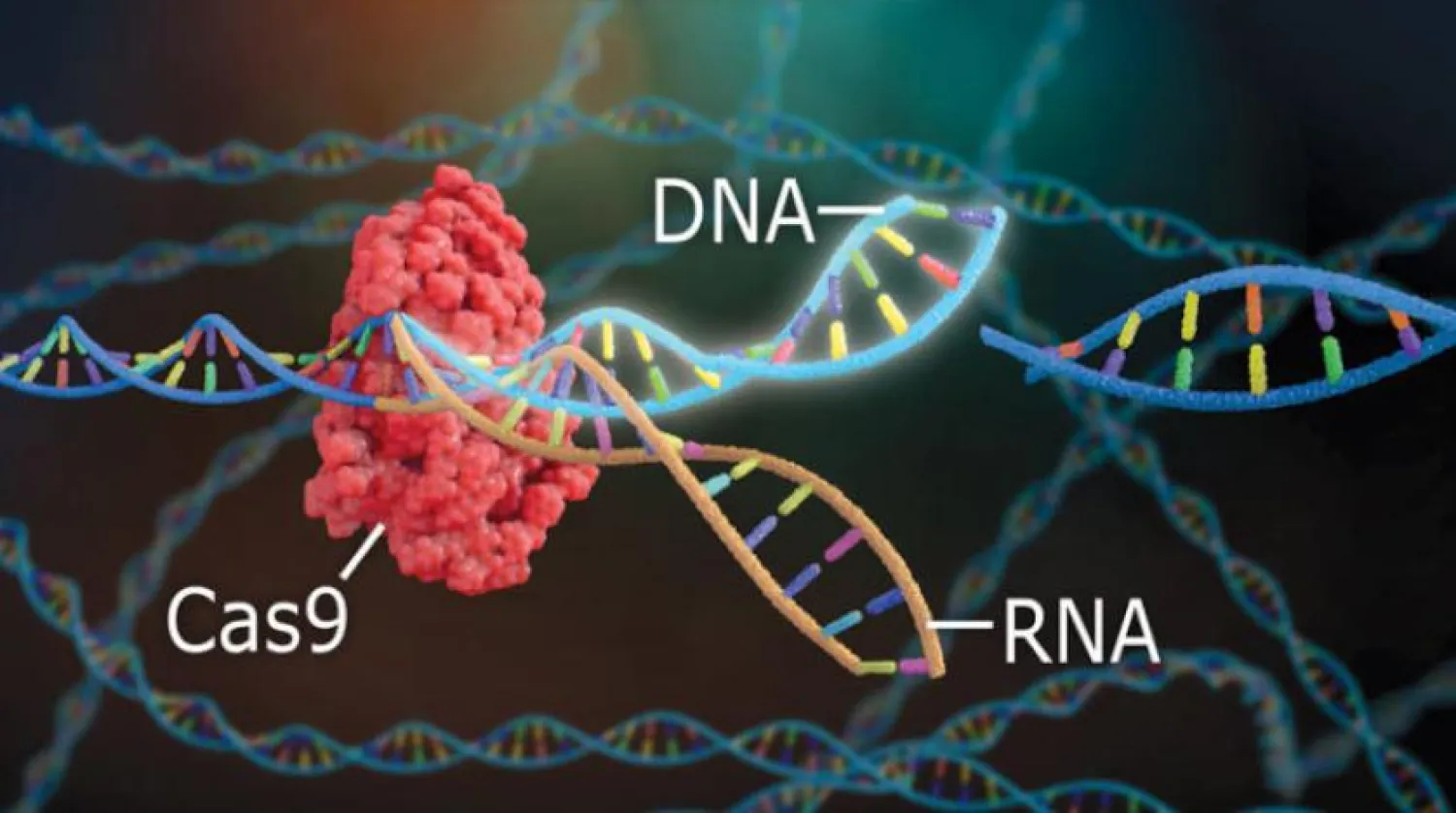
CRISPR-Cas9 tekniğin, bu yüzyılın en önemli bilimsel gelişmelerinden biri olarak görülüyor. CRISPR-Cas9, DNA dizilimlerini ve genlerin görevlerini kolayca değiştirilmesini sağlayarak gen düzenlenme işlemini daha hızlı, doğru, ucuz ve kolay hale getiren güçlü bir araç olarak ön plana çıkıyor. ‘Kümelenmiş düzenli aralıklı kısa palindromik tekrarları’nın kısaltılmış hali olan CRISPR kelimesi, DNA’ların uzantılarından oluşuyor. Cas9 ise kusurlu genlerden kurtulmak için DNA zincirlerini belirli noktalarda keserek moleküler makas görevi gören bir enzim. Bu teknik geliştirilirken, bakteri ve arkelerin viral saldırılarını engellemeye yönelik doğal savunma sisteminden ilham alınmıştı.
CRISPR tekniği, bazı hastalıkları tedavi etmek, yayılmalarını engellemek veya tehlikeli mutasyonları düzelterek hastalığa karşı koruma sağlamak için genetik kusurların düzeltilmesini sağlamıştı. Ayrıca bir dizi genetiği değiştirilmiş yeni bitki ve hayvan üreterek mahsulleri iyileştirebilmesi ile biyoloji dünyasında paradigmaların değişmesine neden olmuştu. Ancak bu teknoloji ahlaki, politik ve patentlerle ilgili tartışmalara neden oluyor. Ayrıca bazı riskler de taşıyor.
Söz konusu risklerden biri, CRISPR-Cas9 enziminin, genomda birkaç noktada istenmeyen veya hedef dışı etkilere neden olması. Örneğin, bazı durumlarda DNA’da çift kesim işlemi yapılması, istenmeyen genetik materyallerin eklenmesine veya büyük ve beklenmedik silinmelerin olmasına neden olabiliyor. Böyle bir durum da kanser gibi olumsuz sonuçlara yol açabiliyor.
Almanya’daki Max Planck Patoloji Bölümü Direktörü Profesör Emmanuelle Charpentier ve ABD’deki Kaliforniya Üniversitesi’nden Profesör Jennifer Doudna, CRISPR-Cas9 veya Genetik DNA Makası olarak bilinen gen düzenleme yöntemini geliştirmeleri sebebiyle 7 Ekim 2020’de Nobel Kimya Ödülü’ne layık görüldüler.
Şu an bazı genetik hastalıkların tedavisinde CRISPR tekniğinin kullanımının güvenliğini test etmek üzere klinik denemeler devam ediyor.
Mutasyonların gözlemlenmesi
KAUST’ta biyoloji bilimleri doçenti olan ve çalışmayı yöneten biyolog Dr. Mo Li çalışmaya dair şu açıklamada bulundu:
“Çalışmamız, CRISPR-Cas9 gen düzenleme yönteminin kullanılmasıyla bağlantılı olan risklerin olabileceği ihtimalini gösteriyor. Gen düzenlemenin sonuçlarını daha iyi araştırmamız için yeni araçlar sağlıyor.”
KAUST ekibi tarafından geliştirilen IDMseq teknolojisi, hücre örneğindeki her bir DNA molekülüne ayrı bir sıra kodlama eklenmesini sonrasında polimeraz zincirleme tepkimesi (PCR) teknolojisi kullanılarak her molekülün çok sayıda kopyasının üretilmesini sağlıyor. Kopyalanan moleküller, orijinal moleküllerle aynı kodlamaya sahip oluyor. (Polimerizasyon reaksiyonu tekniği, belirli bir RNA örneğinin milyarlarca kopyasının hızlı bir şekilde üretilmesi için moleküler biyolojide yaygın olarak kullanılan bir yöntem.)
Bu aşamaların ardından Uzun Okuma Özellikli Moleküler Tanımlayıcı (VAULT) ile Değişken Analizi ve Değişken Analizi isimli biyoinformatik sistem araçları kullanılıyor. Ardından DNA sarmalının kodu çözülüyor ve orijinal DNA molekülleri kaplarının yerlerine benzer moleküller yerleştiriliyor. VAULT teknolojisi, DNA sarmalındaki mutasyonları tespit etmek için bir dizi algoritma kullanıyor. Bu süreç, üçüncü nesil uzun okuma dizilim teknolojileri ile kullanıldığında olumlu sonuçlar veriyor Aynı zamanda bilim adamlarının DNA’da değişiklik ya da orijinal DNA moleküllerindeki büyük miktarda silme ve eklemelerinde her tür mutasyonu belirlemelerini ve sıklıklarını gözlemlemelerine yardımcı oluyor.
Üçüncü nesil uzun okuma teknikleri ile kullanılan bu teknik, 1:100, 1:1000 ve 1:10000 oranlarında, kasıtlı olarak yapılan ve bir grup benzer tür hücre ile karıştırılan bir genetik mutasyonu ortaya çıkarmada başarılı oldu. Ayrıca mutasyonun sıklığını da doğru bir şekilde belirlemeyi başardı.
Ekip, gen düzenleme tekniği CRISPR-Cas9’un yol açtığı mutasyonları taramak için IDMseq’i kullandı. KAUST’ta doktora öğrencisi olan Chun Wei Pai şu açıklamalarda bulundu:
“Güncel bazı çalışmalar, CRISPR-Cas9 ile düzenlenen genlerin etrafında büyük ve beklenmedik silmelere neden olabileceğini ortaya koydu. Bu durum söz konusu teknolojinin kullanılabilirliği konusunda bazı endişelere neden oluyor. Mevcut DNA dizilimi yöntemlerini kullanarak silinen bölümleri belirlemek ve ölçmek zor bir işlemdir. Ancak farklı dizilim platformları ile geliştirdiğimiz yöntem, DNA’daki bu büyük mutasyonları yüksek bir doğruluk oranı ile analiz etmeye yardımcı oluyor.”
Testler, CRISPR-Cas9’un kullanımında gen düzenlemede büyük oranlı silme olaylarının yüzde 2,8 ila 5,4 arasında olduğunu gösterirken genetik olarak düzenlenmiş kısımda tekli DNA mutasyonlarında üç kat artış olduğunu da gösterdi.
Araştırmaları KAUST tarafından finanse edilen uluslararası araştırma görevlisi, Pekin Üniversitesi’nden Profesör Yann Yi Huang “Bu sonuçlar, CRISPR-Cas9 tıbbi tesislerde kullanım için güvenli hale gelmeden önce hakkında öğrenecek çok şeyin olduğunu gösteriyor” dedi.
Araştırmacılar, IDMseq’in şu an tek sarmallı DNA’yı sıralamak için kullanıldığını, çift sarmallı DNA’yı sıralamak için de kullanılmasının tekniğin verimliliğini artırabileceği görüşündeler.